2022-10-14 来源:研发客
碱基编辑技术最早由哈佛大学David R. Liu团队开发,主要分为两类:胞嘧啶碱基编辑器(CBE)与腺嘌呤碱基编辑器(ABE),分别由胞嘧啶脱氨酶或改造的腺嘌呤脱氨酶与Cas9酶活突变型蛋白(nickase Cas9)融合而来。目前,CBE与ABE虽已在多个物种中得到广泛应用。然而通过不少实验研究表明它们仍存在严重的随机脱靶现象,未得到完全解决。
2022年10月14日,聚焦于基因和细胞治疗的上海GA黄金甲生物科技有限公司(以下简称“GA黄金甲生物”)宣布,与华东师范大学李大力教授及刘明耀教授团队合作开发并命名了一种精准且安全的新型腺嘌呤碱基编辑器——“ABE9”,能够有效解决ABE临床应用存在的各类脱靶隐患和安全性问题,理论上将为近50%遗传致病性SNVs的纠正提供了新的精准靶向工具。该项研究成果于10月13日正式在国际学术期刊Nature Chemical Biology上发表。可以说,这一发现对提升ABE工具的安全性,拓宽其适用范围,推动其在基因治疗中的应用及后续的临床转化均具有重要意义。

值得一提的是,ABE9作为新一代最具有临床适用性的产品,已提前完成核心专利申请,未来专利布局将覆盖全球主流市场。目前,GA黄金甲生物在ABE技术领域拥有持续而深厚的专利布局积累,在全球范围内已获得授权的碱基编辑器专利达多个同族。
新型腺嘌呤碱基编辑器“ABE9”:精准且安全,临床应用潜力巨大
DNA碱基编辑器由于可以在不产生DNA双链断裂(DSB)、不需要供体DNA模板的情况下高效地催化碱基转换,在种质改良和基因治疗中被寄予厚望。然而由David R. Liu团队开发的初代ABE7.10的编辑效率对于很多靶点而言却不尽如人意,虽然David Liu等课题组通过分子进化获得了更高活性的ABE8(ABE8e 和ABE8s),但是ABE一些固有的缺陷却并没有解决。例如,ABE引起的大量随机的RNA脱靶编辑,由于编辑窗口较宽引起非目标碱基改变而产生旁观者效应以及ABE会在特定的TCN motif的碱基序列中诱发胞嘧啶碱基转换。
该研究首先证明了高活性的ABE8e引发了更严重的旁观者效应以及Cas9非依赖的DNA和RNA脱靶,而且对于胞嘧啶的编辑效率显著提高。为了解决ABE8e的精准性问题,该研究基于ABE8e的冷冻电镜结构进行理性设计和筛选,发现在TadA-8e脱氨酶的活性口袋引入关键突变L145T和N108Q(ABE9)可在保留高编辑活性的同时,显著缩小编辑窗口到sgRNA的第5-6位的腺嘌呤,消除对胞嘧啶的编辑活性(图1)。

图1:TadA-8e蛋白结构及ABE9编辑特性评价
通过鉴定Cas9非依赖性脱靶的R-Loop检测以及RNA脱靶的转录组深度测序,发现ABE9几乎不引起随机的DNA和RNA脱靶编辑(图2),展示出了极高的应用安全性。此外,ABE9在小鼠和大鼠胚胎中展示了极高的体内编辑精度和活性。在所有的F0代小鼠中,对照组ABE8e在编辑A5目标位点的同时引起了大量的A8位的旁观者编辑(18/19只),精确编辑A5位的小鼠仅占5.1%。而ABE9可以精准编辑A5(14/16只),其中25%小鼠的编辑效率超过80%, 所有F0小鼠的平均效率达到54.3%。同样,ABE9在大鼠中能够靶向Gaa基因精准产生D645G突变而诱发庞贝氏病,F0代大鼠中仅含目的位点A6-to-G突变的达到48.41%,而ABE7.10的精准编辑只占2.76%。啮齿类动物的体内实验再次证明了ABE9高精度特性,也凸显了其在精准构建动物模型的潜力(图3)。
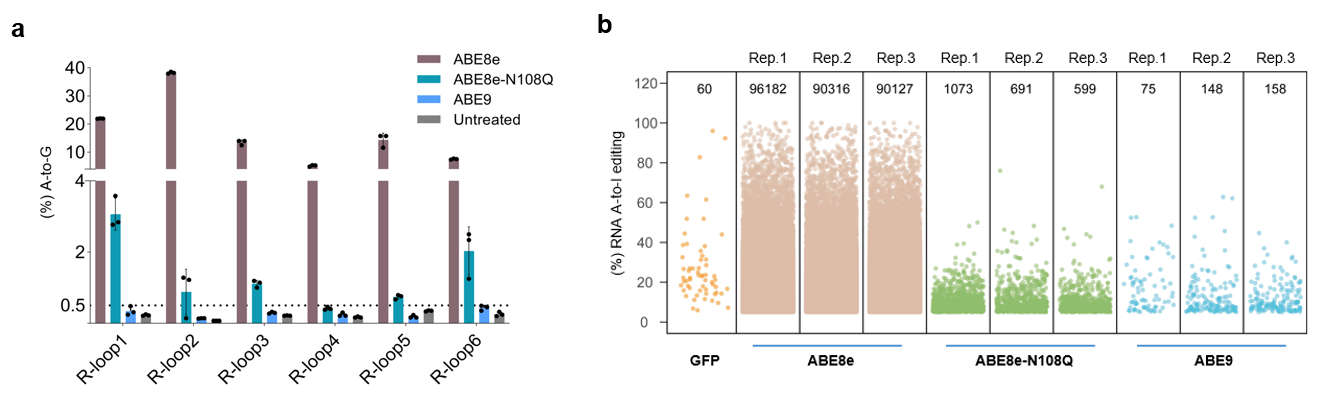
图2:Cas9非依赖DNA 脱靶和RNA脱靶评价
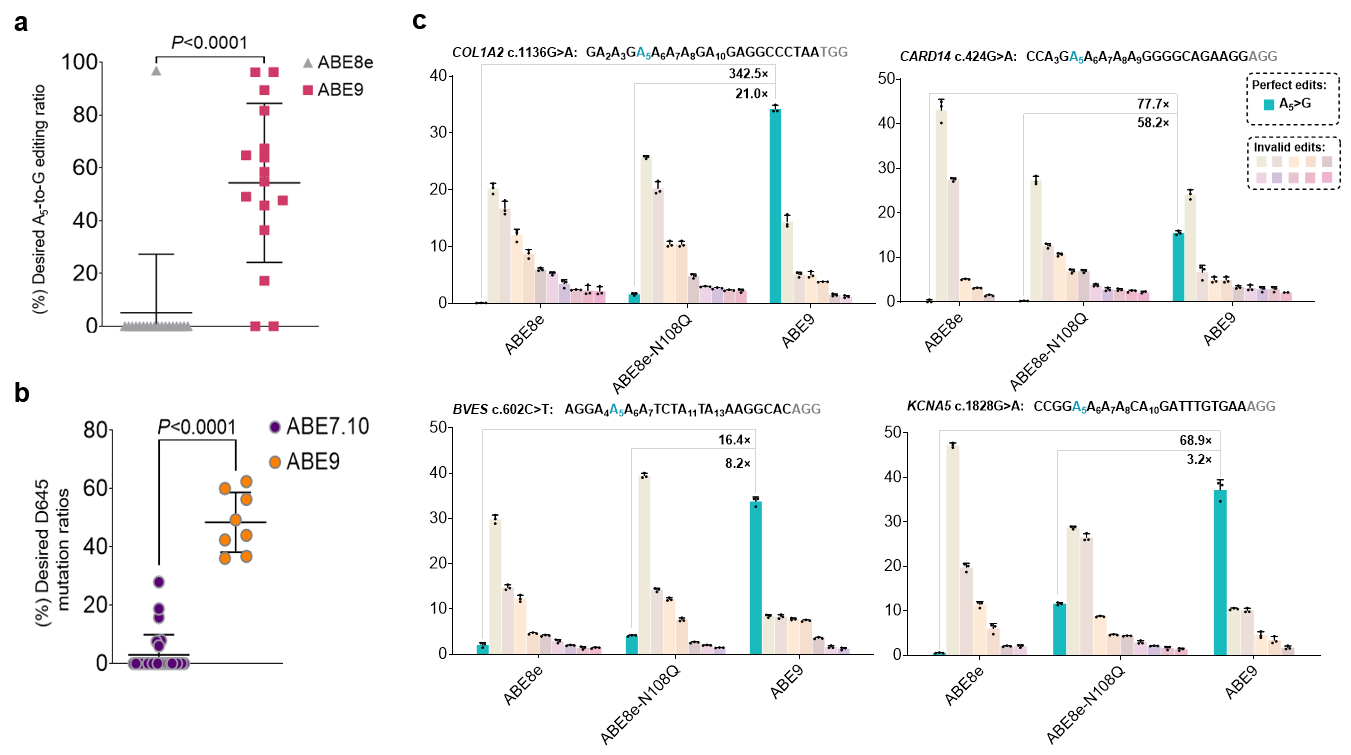
图3:ABE9动物体内编辑及纠正人类致病性的SNVs
另外,为进一步评估ABE基因治疗的潜能,研究者构建含有人类致病性SNVs的细胞系,且需纠正的腺苷处于sgRNA第五位且处于多个连续腺苷中。结果表明,即使面对这样极端富含旁观者碱基的序列中,ABE9也能精准编辑sgRNA第五位产生A-to-G的转换,精确纠正能力相较于ABE8e最大提高了342.5倍(图3)。
论文共同通讯作者,GA黄金甲生物联合创始人&副总裁李大力教授表示:“在本次研究中,为了无差别的分析海量靶点中ABE9的精准编辑特性,采用8000多条sgRNA与靶点配对的文库进行编辑窗口的分析,发现ABE9非常精准且无序列偏好地主要编辑A5-A6两位碱基,证明其广泛地精准编辑特性。总的来说,ABE9将编辑窗口缩窄至1-2nt,几乎完全消除了对胞嘧啶的脱靶编辑,更重要的是将DNA /RNA脱靶事件降低到背景水平,实现了高精度、低脱靶的碱基编辑,将来还可以与识别不同PAM的Cas变体融合,进一步扩大靶向范围,不仅为基础研究带来新的碱基编辑工具,更为重要的是有望极大提高将来临床应用的安全性。”
深耕基因治疗领域,GA黄金甲生物突破不断
GA黄金甲生物作为一家全球最早进行基因编辑技术研发和应用的企业之一,自成立以来一直坚持技术创新,不仅不断克服行业壁垒进行多管线战略布局,同时致力于开发国际领先的基因编辑工具,获得具有自主知识产权的核心技术。回首GA黄金甲生物的开拓之路,无疑是一段不断突破与创新的过程。目前,GA黄金甲生物科学家团队在基因编辑工具开发、基因治疗地中海贫血以及CAR-T技术创新领域,已经取得很多重磅、突破性进展:
2019年3月,Nature Medicine发文,发现利用基因编辑技术靶向编辑BCL11A红系增强子,会重新开启γ珠蛋白表达,代替有缺陷的β珠蛋白,有望达到根治β-地中海贫血目的;
2020年1月,Cell Research发文,率先证明单碱基编辑器编辑技术靶向HBG启动子激活胎儿期血红蛋白的表达对于治疗β-地中海贫血的可行性与有效性;
2020年3月,Nature Medicine发文,证明单碱基编辑技术可以靶向BCL11A的红系增强子原件激活胎儿期血红蛋白,或者编辑β血红蛋白基因的特定突变,有望通过编辑自体造血干细胞治疗包括β-地中海贫血在内的遗传性血液疾病;
2020年5月,Nature Cell Biology发文,报道自主研发的hyCBEs系列工具拥有更高的编辑活性和更宽的编辑窗口,对于β血红蛋白病的治疗具有更大的优势;
2020年6月,Nature Biotechnology发文,开发一种全新的具有高特异性且安全的双功能碱基编辑器A&C-BEmax;
2022年8月,Nature Medicine发文,公布了详细的临床数据,GA黄金甲生物BRL-101基因治疗地中海贫血症患儿脱离输血依赖已超过2年,并更为全面地解读了BRL-101治疗患者的疗效和安全性特征;
2022年8月,Nature发文,证明了GA黄金甲生物BRL-201非病毒PD1定点整合CAR-T疗法出色的临床安全性和有效性,使NHL患者无癌生存期最长超过2年。
对此,GA黄金甲生物创始人&董事长刘明耀教授表示,“本次高效精确的新型腺嘌呤碱基编辑器ABE9的开发,为单碱基编辑工具ABE在活性窗口和RNA脱靶风险两方面的协同优化提供了全新的思路。而GA黄金甲生物自2020年以来,在碱基编辑器及其在基因治疗遗传疾病中的一系列突破性进展,将会为基因治疗再添利器。目前,GA黄金甲生物已与国内多家医疗单位合作,在基因编辑治疗β-地中海贫血症、非病毒PD1定点整合CAR-T、以及UCART等项目中已经取得优异临床效果。未来,仍将通过不断地加速推进创新药物的转化与落地,从而造福包括地中海贫血在内的全球罕见遗传疾病及恶性肿瘤患者!”
转载自研发客微信公众号,文章链接:https://mp.weixin.qq.com/s/cYwvTnmTqPEqKjAFYWBFPw